Roman Vuerich - Corso di Dottorato in Biomedicina molecolare
Non tutto il grasso vien per nuocere – una nuova terapia di medicina rigenerativa per le ferite difficili
Promozione della rivascolarizzazione delle ferite ischemiche attraverso la formazione di vasi ibridi tra donatore e ricevente
Le ferite difficili sono lesioni cutanee dolorose che non guariscono e spesso peggiorano nel tempo. Ciò è tipicamente causato dalla coesistenza di patologie croniche sottostanti, come il diabete e le arteriopatie periferiche, che impediscono un'adeguata vascolarizzazione della ferita. Senza un sufficiente apporto di ossigeno e nutrienti da parte del sangue, la ferita non può guarire correttamente.
Si tratta di una condizione comune nelle persone di età superiore ai 60 anni, almeno tanto quanto l'insufficienza cardiaca, con limitazioni significative nelle attività quotidiane. Inoltre, l'incidenza è in aumento a causa dell'incremento dell'età media della popolazione, dei casi di diabete e delle malattie croniche. Le ricadute economiche a causa delle ferite difficili sono considerevoli, con circa il 3% del budget sanitario globale speso per il loro trattamento. Solo in Italia, il costo del trattamento delle ferite difficili ammonta a oltre 3 miliardi di euro all'anno, poiché spesso richiedono terapie specialistiche e costose. In aggiunta, i pazienti con ferite difficili possono subire una riduzione della capacità lavorativa e richiedere un'assistenza sanitaria continua.
Le terapie attualmente disponibili per le ferite difficili prevedono l'uso di sostituti cutanei per promuovere la guarigione della ferita, ma la loro efficacia è ostacolata dalla scarsa vascolarizzazione che tipicamente è alla base di questa patologia. Per affrontare questo problema e promuovere la rivascolarizzazione della ferita, abbiamo sviluppato una nuova terapia che utilizza la frazione vascolare stromale (in inglese – Stromal Vascular Fraction, SVF). La SVF è una popolazione eterogenea di cellule derivate dal grasso che contiene tutti i mattoncini necessari per la formazione di nuovi vasi sanguigni. Per studiare gli effetti terapeutici di questa nuova terapia, abbiamo sviluppato un modello preclinico di ferita ischemica che simula realisticamente la patologia che si verifica nell'uomo. Abbiamo quindi applicato sulla ferita le cellule della SVF prelevate dal grasso sottocutaneo dei pazienti, ottenuto mediante liposuzione.
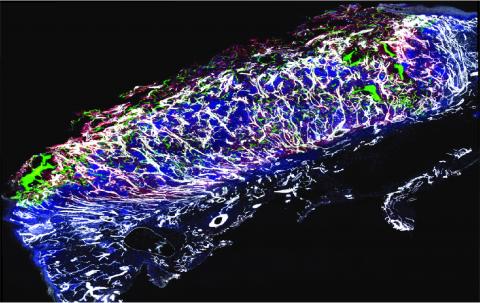
Dopo una sola settimana, le cellule della SVF sono state in grado di formare una nuova rete vascolare funzionale, collegata al flusso sanguigno attraverso i vasi preesistenti nella ferita (Figura in alto a destra). Il ripristino del normale apporto di sangue in seguito alla formazione dei nuovi vasi sanguigni ha accelerato significativamente il processo di guarigione rispetto alle terapie convenzionali e ha permesso la chiusura della ferita dopo sole tre settimane. Inoltre, abbiamo dimostrato che le cellule derivate da pazienti diabetici, che sono il bersaglio principale di questa terapia, possono essere espanse in un bioreattore, preservando il potenziale terapeutico della SVF.
Abbiamo così caratterizzato il duplice meccanismo d'azione della nostra terapia. Da un lato, le cellule che compongono i vasi della SVF si sono innestate ed espanse nel letto della ferita, contribuendo direttamente alla formazione di nuovi vasi. Dall’altro lato, una popolazione di progenitori fibro-adipogenici produceva dei fattori di crescita che supportavano ulteriormente l'espansione e la funzione della nuova vascolarizzazione. Questi dati hanno importanti implicazioni cliniche, in quanto rappresentano un passo avanti verso l'adozione riproducibile ed efficace della SVF come cura standard per le ferite difficili.